khi nung tinh thể đồng II sunfat ngậm nước để khử nước kết tinh, khối lượng tinh thể giảm 36%. xđ ctpt tt trên
giúp mk vs ạ !!! mk cần gấp
Trong tinh thể ngậm nước của muối sunfat KL hoá trịII, nước kết tinh chiếm 45,324% khối lượng tinh thể chứa 11,51% lưu huỳnh. Xác định công thức của tinh thể
1/ Trong tinh thể ngậm nước của một muối sunfat kim loại hóa trị (II), nước kết tinh là 45,32% về khối lượng. Xác định công thức phân tử của tinh thể, biết tinh thể chứa 11,51% là lưu huỳnh về khối lượng.
2/Y là một oxit kim loại chứa 70% kim loại về khối lượng . Tìm công thức phân tử của Y.
1/ CTHH dạng TQ là ASO4 . xH2O
*Có : %S/muối tinh thể = \(\dfrac{1.M_S}{M_{ASO4.xH2O}}.100\%=11,51\%\)
=> \(\dfrac{32}{M_{ASO4.xH2O}}=0,1151\)
=> MASO4.xH2O = 278(g)
* Có : %H2O/muối tinh thể = \(\dfrac{x.M_{H2O}}{M_{ASO4.xH2O}}.100\%=45,32\%\)
=> \(\dfrac{x.18}{278}=0,4532\)
=>x= 7
*Lại có : MASO4.xH2O = 278
mà x = 7
=> MA + 96 + 7 .18=278 => MA =56(g) => A là Sắt (Fe)
Vậy CTPT của tinh thể là FeSO4 .7H2O
A là công thức phân tử của tinh thể ngậm nước CuSO4.nH2O trong đó chứa 36% lượng nước kết tinh.
a) Xác định công thức phân tử của A?
b) cần bao nhiêu g tinh thể A và bao nhiêu g tinh thể CuSO4 8% để khi trộn vào nhau thì thu được 280g dd CuSO4 16%
A là công thức phân tử của tinh thể ngậm nước CuSO4.nH2O trong đó chứa 36% lượng nước kết tinh.
a) Xác định công thức phân tử của A?
b) cần bao nhiêu g tinh thể A và bao nhiêu g tinh thể CuSO4 8% để khi trộn vào nhau thì thu được 280g dd CuSO4 16%
trong thành phần của 1 muối nitrat ngậm nước của kim loại hóa trị II thì khối lượng nước kết tinh =42,1875% khối lượng kim loại =9,375%% xác định tinh thể
CTHH: R(NO3)2.xH2O (A)
\(\%m_{NO_3^-}=100\%-42,1875\%-9,375\%=48,4375\%\)
Xét \(\dfrac{m_R}{m_{NO_3^-}}=\dfrac{1.M_R}{2.62}=\dfrac{9,375\%}{48,4375\%}\)
=> MR = 24 (g/mol)
=> R là Mg
(A) có CTHH là Mg(NO3)2.xH2O
Có: \(\%m_{H_2O}=\dfrac{18x}{148+18x}.100\%=42,1875\%\)
=> x = 6
=> CTHH: Mg(NO3)2.6H2O
Một muối sunfat của kim loại hóa trị II ngậm nước có phân tử khối 278 gam và khối lượng nước kết tinh chiếm 45,324%. Tìm công thức hóa học của muối trên.
Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
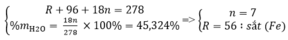
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O
Trong tinh thể muối sunfat hóa trị II nước kết tinh chiếm 45,34% về khối lượng và tinh thể chứa 11,5%S.Xác định công thức hóa học của tinh thể
1/ CTHH dạng TQ là ASO4 . xH2O
%S tinh thể =\(\frac{1.M_S}{M_{ASO4.xH2O}}.100\%=11,5\%\)
=> \(\frac{32}{M_{ASO4.xH2O}}=0,115\)
=> MASO4.xH2O = 278(g)
% H2O kết tinh = \(\frac{x.M_{H2O}}{M_{ASO4.xH2O}}.100\%=45,34\%\)
=> \(\frac{x.18}{287}=0,4534\)
=>x= 7
MASO4.xH2O = 278
mà x = 7
=> MA + 96 + 7 .18=278
=> MA =56(g) => A là Sắt (Fe)
Vậy CTPT của tinh thể là FeSO4 .7H2O
Chúc bạn học tốt
một tinh thể ngậm nước có công thức là M(NO3)3.nH2O, trong đó % khối lượng oxi trong tinh thể là 71,29%, % khối lượng hidro là 4,46%
a) tìm công thức tinh thể
b) tìm thể tích khí NH3 để chứa được lượng nitơ bằng lượng nitơ trong 8,08 gam tinh thể trên
Cho muối sunfat ngậm nước trong phân tử có 1 số nguyên phân tử nước. PTK của muối ngậm nước là 666đ.v.c. Biết rằng S chiếm 14,415%. Cho dd chứa 6,66g muối ngậm nước tác dụng đủ vs NaOH loãng lọc rửa kết tủa hiddroxit lim loại đem nung đc 1.02g một chất k bay hơi. Hỏi đó là muối k loại nào Viết ct tinh thể